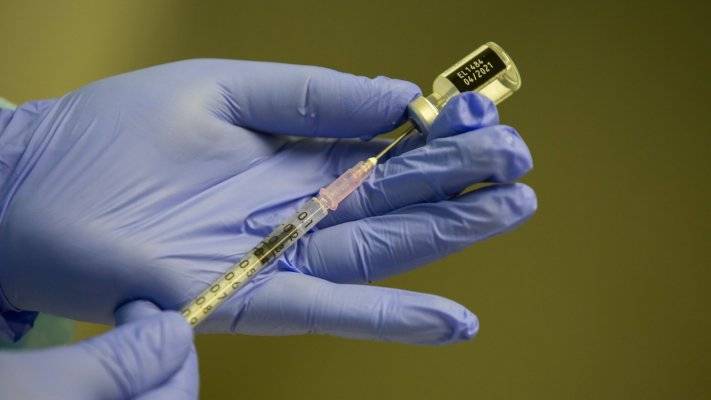
“A meio deste ano, poderemos iniciar os ensaios clínicos [depois de os ensaios pré-clínicos que estão ainda a decorrer] e depois, em nove meses, ter os resultados para pedir uma autorização de emergência, tal como foi feito com as vacinas que estão no mercado”, disse à agência Lusa o diretor-executivo da Immunethep, Bruno Santos, apontando para o final do primeiro semestre de 2022 a altura em que a vacina poderá estar pronta para a sua produção e distribuição.
No entanto, esses prazos só poderão ser cumpridos caso a Immunethep, sediada no Biocant Park, em Cantanhede, no distrito de Coimbra, receba investimento por parte do Estado para tornar o processo o mais rápido possível.
“Sem isso, o prazo será muito mais estendido. O atraso na entrada de capital irá refletir-se no resultado de quando a vacina estará no mercado”, explicou, referindo que são necessários cerca de 20 milhões de euros, caso as entidades reguladoras aprovem o plano de ensaios clínicos.
Segundo Bruno Santos, a Immunethep já tem vários privados interessados em investir no desenvolvimento da vacina, mas só o irão fazer quando tiverem “uma perspetiva mais clara sobre o interesse nacional em apoiar esta vacina”.
“O volume de investimento que é necessário é difícil de mover em privados. Era mais rápido se o investimento fosse público. Tivemos uma pequena ajuda do Portugal2020, em que recebemos 250 mil euros, mas a Pfizer recebeu 250 milhões do Estado americano. Tentar fazer algo, com mil vez menos, é impossível”, frisou.
De acordo com o responsável, o interesse privado em apoiar a produção da vacina centra-se também na possibilidade de a mesma ser usada, “por exemplo, nos PALOP [Países Africanos de Língua Oficial Portuguesa], que terão muito mais dificuldade de acesso à vacina]”.
A vacina desenvolvida pela empresa sediada no Biocant apresenta “algumas características diferenciadoras”, notou.
Ao contrário das vacinas da Moderna e da Pfizer que identificam apenas uma parte importante do vírus, uma proteína, a da Immunethep usa “o vírus como um todo”, o que a torna mais abrangente perante variantes do novo coronavírus.
Por outro lado, como a vacina será administrada por inalação, permite uma “maior proteção dos pulmões, que é onde entra o vírus”, e uma maior facilidade na sua distribuição e administração, por não exigir “nem temperaturas negativas nem um profissional de saúde que saiba administrar por via intramuscular”, aclarou.
A empresa biotecnológica fundada em 2014 tem já acordos de produção, nomeadamente com uma empresa especialista sediada no Canadá, estando também a avaliar a possibilidade de se “trazer uma unidade de produção de vacinas para Portugal”, referiu.